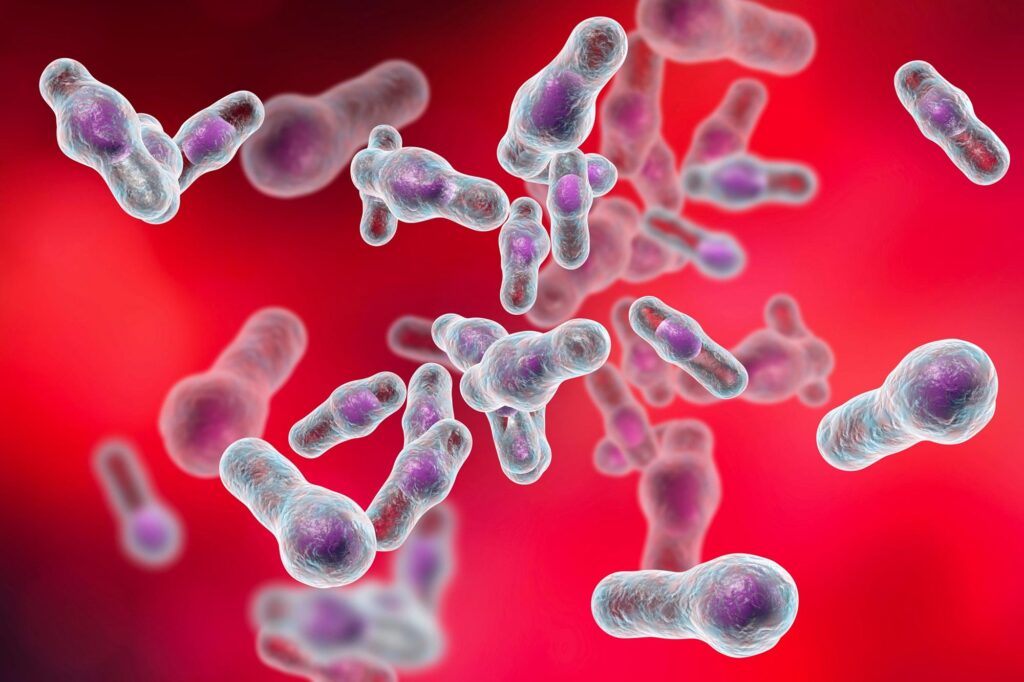
El biólogo Joseph Sorg dirige un equipo para analizar C. difficile, que mata al menos a 29.000 personas al año.
Científicos de todo el mundo han estado trabajando seriamente para mejorar la comprensión de una superbacteria cada vez más virulenta, Clostridium difficile .
El patógeno altamente contagioso generalmente adquirido en el hospital, designado por los Centros para el Control y la Prevención de Enfermedades como una de las cinco amenazas más urgentes para el sistema de salud de los EE. UU., Causa más de 500,000 infecciones y 29,000 muertes cada año a un costo social total que excede los $ 5 mil millones de dólares en ese país.
Los biólogos de la Universidad de Texas A&M y la Facultad de Medicina de Baylor se han asociado en un nuevo estudio de biología de sistemas financiado por los Institutos Nacionales de Salud con el objetivo de abordar el problema en su origen, el punto inicial de infección, con la esperanza de identificar qué hace que los pacientes sean susceptibles a ella, en primer lugar.
Estudios anteriores han demostrado que la infección por C. difficile está fuertemente correlacionada con una gran abundancia de ácidos biliares secundarios que son tóxicos para Clostridium difficile en entornos de laboratorio.
Estas pequeñas moléculas son generadas por un microbioma intestinal sano a partir de ácidos biliares primarios que se sintetizan en el hígado.
El biólogo de Texas A&M y becario EDGES, Joseph Sorg, dice que los científicos han visto durante mucho tiempo estas pequeñas moléculas como un protector clave para prevenir la infección por Clostridium difficile
La investigación fue presentada por primera vez por la estudiante graduada del Laboratorio Sorg Andrea Martinez Aguirre en un artículo publicado a principios de este otoño en la revista PLOS Pathogens con la ayuda del grupo de Tor Savidge en Baylor College of Medicine.
“Muchos esfuerzos en curso están desarrollando opciones de tratamiento con probióticos para pacientes infectados con Clostridium difficile , esfuerzos que se enfocan en restaurar los ácidos biliares secundarios a los pacientes”, dijo Sorg. “Nuestros hallazgos muestran que estos tratamientos deberían centrarse en cambio en los microbios que consumen nutrientes importantes para el crecimiento de Clostridium difficile y que los ácidos biliares secundarios son una pista falsa para la protección”.
Como base de su estudio, el equipo utilizó ratones derivados libres de gérmenes en el Baylor College of Medicine que fueron colonizados con una sola especie de bacteria que se sabe está involucrada en la generación secundaria de ácidos biliares y está fuertemente correlacionada con un ambiente protector de Clostridium difficile .
Como medida de control adicional, seleccionaron una cepa de ratón mutante comprada a través del Proyecto Knockout Mouse de los NIH que se crió en Texas A&M y se distingue por su incapacidad para sintetizar una clase importante de ácidos biliares, lo que limita aún más la reserva de ácidos biliares secundarios.
“Sorprendentemente, encontramos que los ratones colonizados con estos microbios ( C. scindens , C. hiranonis o C. leptum ) protegían contra la enfermedad de Clostridium difficile pero no producían ácidos biliares secundarios”, dijo Sorg.
Sorg se unió al Departamento de Biología de Texas A&M en 2010 y ha estado trabajando desde sus días postdoctorales para descubrir la ciencia básica de Clostridium difficile, desde su fisiología hasta su virulencia.
Obtuvo su doctorado en microbiología en la Universidad de Chicago en 2006, el mismo año en que se secuenció el genoma de Clostridium difficile , y desde entonces se ha convertido en uno de los pioneros del estudio de C. difficile .
Referencia: “Bile acid-independent protection against Clostridioides difficile infection” by Andrea Martinez Aguirre, Nazli Yalcinkaya, Qinglong Wu, Alton Swennes, Mary Elizabeth Tessier, Paul Roberts, Fabio Miyajima, Tor Savidge and Joseph A. Sorg, 19 October 2021, PLOS Pathogens.
DOI: 10.1371/journal.ppat.1010015